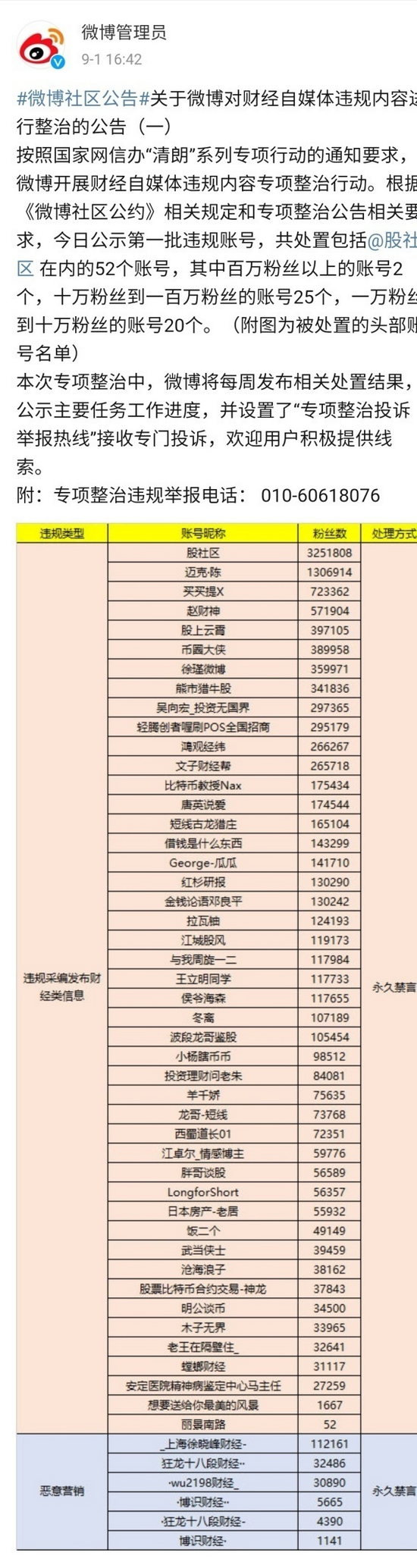
原标题:重磅新药“狗抗”上市申请遭拒,华北制药为何说成“自主撤回”
 图片来源:视觉中国
图片来源:视觉中国华北制药8月12日晚公告称,其正在上市审评中的重磅新药重组人源抗狂犬病毒单抗注射液(rhRIG)大规格(500 IU/2.5ml,受理号CXSS2000040)“黄了”。二级市场上,华北制药8月13日大跌。早盘低开后,盘中一度跌逾7%。截至收盘,报收10.22元/股,跌6.67%。最新市值仅剩175亿元。
华北制药称,相关原因是公司对临床需求、市场情况、研发成本等因素调研分析后,提出主动撤回,而撤回时间是今年3月。
但今年3月的撤回申请,为何忽然在8月份公告进行披露?而根据行业媒体医药魔方8月12日晚报道,重组人源抗狂犬病毒单抗注射液的上市申请中受理号CXSS2000040(对应规格:500 IU/ 2.5ml)未获得国家药监局批准,另一个受理号CXSS2000039(对应规格:200IU/1.0ml)目前处于1轮发补阶段。
从时间上看,在华北制药称自己“提出主动撤回”是在今年3月,但今年4月30日,国家药监局食品药品审核查验中心发布的药品注册申请生产现场检查任务信息公告还显示,对华北制药该产品的两个受理号:CXSS2000039、CXSS2000040同时进入药品注册现场检查。
 图片来源:药品注册申请药学研制和生产现场检查任务信息公告(2021年第9号)
图片来源:药品注册申请药学研制和生产现场检查任务信息公告(2021年第9号)但如果华北制药已经撤回申报了,药审中心为何还会进行现场检查呢?界面新闻记者从丁香园Insight医药情报助手上查询则发现,在今年3月后,这个受理任务依然在继续,8月2日,CXSS2000040受理号状态变更为“在审批”。
而Insight医药情报助手还显示,在8月10日时,药审中心对CXSS2000040任务做出了“未被批准”的审评结论。而这些显然都与华北制药公告说法存在大量矛盾之处。

丁香园Insight医药情报助手上“狗抗”的审评任务时光轴
退一步来看,如果按照华北制药所言,公司在今年3月便申请了撤回,为何其当时却没有进行公告。
在今年7月30日,针对投资者在互动平台上问的“贵司狂犬单抗的生产现场检查结束了没有?”华北制药当时还曾回答:“公司重组人源抗狂犬病毒单抗注射液注册报批事项正有序推进中,公司将密切关注该项目的后续进展,并严格按照相关法律法规及时履行信息披露义务。”
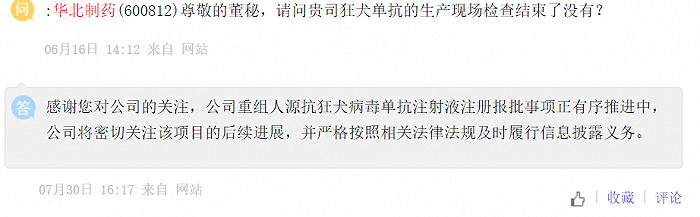 图片来源:上证e互动。
图片来源:上证e互动。而这一事件的诸多疑点,不仅让人联想起近年上半年康弘药业暂停核心品种康柏西普的海外临床试验一事,两者在说法、时间线上均存在类似的矛盾之处。
对于当前的大规格产品的“突发式主动撤回”事件,界面新闻多次拨打该公司董秘办电话,均未能接通。采访邮件也未获得书面回复。
而华北制药在公告则称,待公司取得国家药品监督管理局签发的相关撤回申请审批文件后,将及时披露所涉及的药品信息、药品研究相关情况、项目投入、以及市场状况等有关详细情况。
华北制药曾是我国最大抗生素生产企业。其主要从事医药产品的研发、生产和销售等业务,公司产品涉及化学药、生物药、营养保健品等,治疗领域涵盖抗感染药物、心脑血管药物、肾病及免疫调节类药物、肿瘤治疗药物、维生素及营养保健品等近700个品规。
2009年,冀中能源入主华北制药,曾提出由生产青霉素向头孢转型,培育新的利润增长点。此后,受环保压力及限抗令影响,该公司又提出产品结构从原料药为主向制剂药方向转型。不过,种种迹象显示,如今盈利增长远不如营收,2020年利润主要来源于“政府补贴”的经营窘境。
而这次受到质疑的新产品,戏称市场为“狗抗”,本是华北制药股东们期待多年的重磅独家品种。
据华北制药此前公告介绍,若“狗抗”将与人用狂犬病疫苗联用,可以用来补充人用狂犬病疫苗主动免疫过程中的抗体空白,从而直接中和体内狂犬病毒,起到被动免疫作用。因此,其被期待用于被狂犬或其它狂犬病毒易感动物咬伤、抓伤患者的被动免疫。截至彼时,国内尚无重组抗狂犬病毒单抗药物上市销售。
2007年华北制药首次了提交了“狗抗”的临床试验申请(200IU/瓶,500IU/瓶两个规格),并于2009年6月25日获得临床试验批件(批件号为2009L06541和2009L06542)。不过,随后该项目的进展缓慢,Ⅰ期临床试验直到2013年10月才完成;Ⅱ期临床试验于2018年4月完成。
2020年4月7日,华北制药取得该项目III期临床试验报告。试验结论为:重组人源抗狂犬病毒单抗注射液(rhRIG)是安全、有效的。当时该项目累计研发投入金额为1.46亿元。
而据华北制药2020年修订版年报显示,2018年-2020年,其分别实现营收97.61亿元、114.57亿元、114.93亿元;实现归母净利润1.69亿元、1.72亿元、0.97亿元。但今年第一季度,公司营收约27.13亿元,同比增长17.08%;归母净利润亏损约5720万元,同比下降185.74%。