图片来源:Pixabay
图片来源:Pixabay撰文|王聪
编辑 | nagashi
排版|水成文
据世界卫生组织(WHO)统计,全球有近20亿人超重或肥胖,每年因超重或肥胖导致的死亡高达280万。在全世界范围内,肥胖已经成为了一个主要公共健康问题。
肥胖者往往会出现高血糖、高血脂,以及高血压,也就是所谓的“三高”。因此他们更容易患心血管疾病和代谢性疾病。
但是科学家已经观察到,有多达45%的肥胖者的血糖、血脂、血压水平处于健康状态,因此他们患病的风险可能并不高。这部分肥胖者保持健康的原因是什么,人们对此还知之甚少。
近日,美国西奈山伊坎医学院和丹麦哥本哈根大学的研究人员在 Nature 子刊 Nature Metabolism 杂志发表了题为:Genome-wide discovery of genetic loci that uncouple excess adiposity from its comorbidities 的研究论文。
该研究对超过30万人进行大规模全基因组关联分析,确定了62个基因位点,其中相同的等位基因与较高的肥胖率和较低的心脏代谢风险显著相关。功能分析表明,这62个基因位点富含脂肪组织中表达的基因,以及影响附近脂肪细胞分化的基因的调控突变体。
这些发现提供了新的生物学思路,可以将体内更高水平的脂肪与更高的糖尿病和心脏病风险分离开来。
更重要的是,这些基因似乎通过帮助维持健康的脂肪组织而对人体健康有益,为开发代谢性疾病和心脑血管疾病提供了新的靶标,有望通过改善脂肪组织的健康状况来降低罹患糖尿病和心脏病的风险。

这是第一个全基因组水平的肥胖与心脏代谢特征的跨表型荟萃分析,研究团队通过分析数十万人的数据,评估这些人的体脂和疾病风险指标。
分析结果确定了基因组的62个位点,这些位点与体内高脂肪含量和较低的心脏代谢疾病风险显著相关。这些基因中的一些可能作为减少与肥胖症相关的心脏代谢风险的治疗靶标。
进一步的分析表明,这些基因在体内具有一系列功能,每个基因位点中排列优先顺序的基因在支持脂肪分布(FAM13A,IRS1和PPARG)和脂肪细胞功能(ALDH2,CCDC92,DNAH10,ESR1,FAM13A,MTOR,PIK3R1和VEGFB)中起关键作用。还涉及其他一些机制,例如胰岛素-葡萄糖信号传导(ADCY5,ARAP1,CREBBP,FAM13A,MTOR,PEPD,RAC1和SH2B3),能量消耗和脂肪酸氧化(IGF2BP2),白色脂肪组织褐变(CSK, VEGFA,VEGFB和SLC22A3)和炎症(SH2B3,DAGLB和ADCY9)。
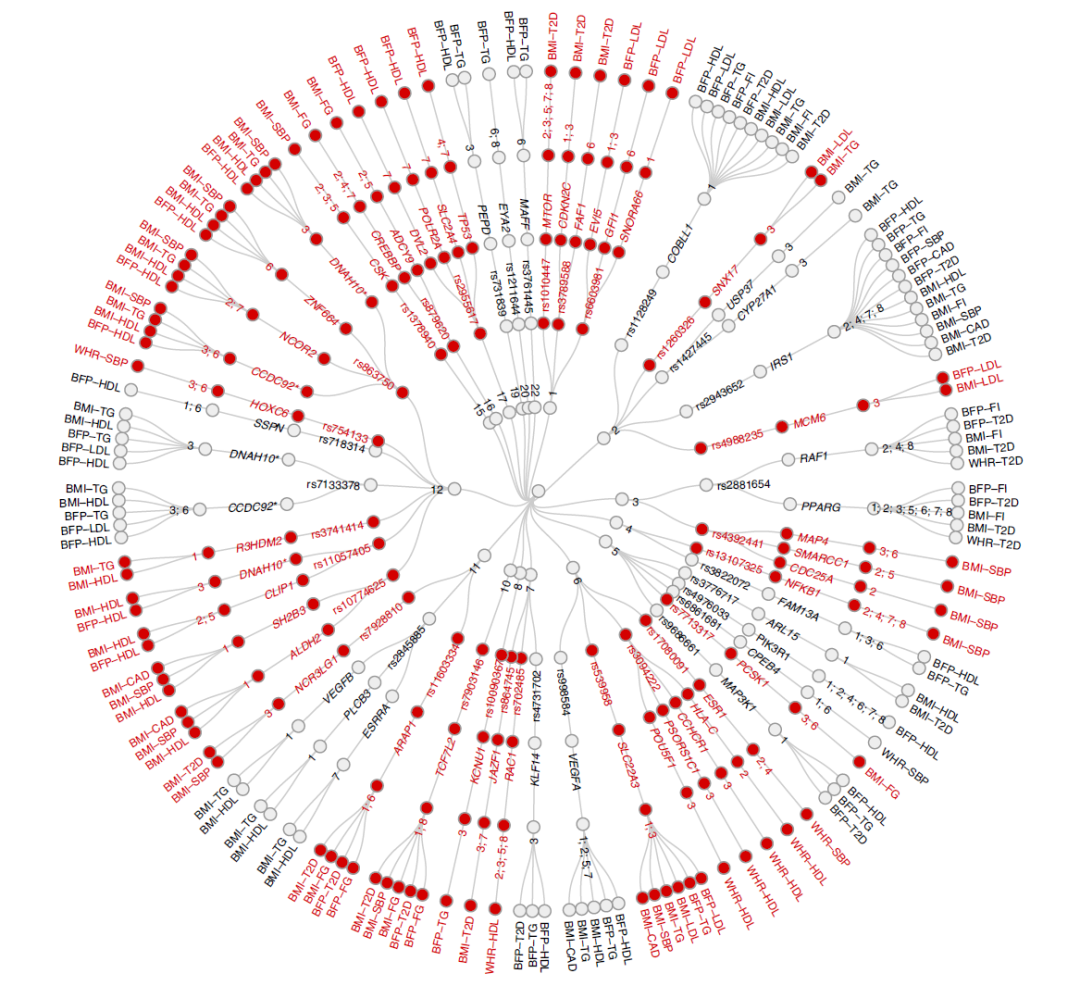
研究团队表示,这项研究发现的是与脂肪组织健康相关的新基因,而不是那些与中枢神经系统相关的已知的肥胖基因,那些与中枢神经系统相关的肥胖基因是通过调控饱腹感影响肥胖,通常与不健康的肥胖有关。
肥胖是一种复杂的疾病,并非每个肥胖的人都同样有患心血管疾病和代谢性疾病的风险。知道哪些基因可以保护人们免受糖尿病和心血管疾病的侵害,最终将帮助人们更好地诊断和治疗肥胖症患者。这项研究也标志着人们朝着更细致入微的肥胖治疗方法迈出了重要一步。