▎药明康德内容团队编辑
人体由万亿级数量的细胞组成,但无论细胞的形态如何,执行着怎样的功能,它们都有着一个共同的特征,一个由双层磷脂形成的保护性膜结构,其也被称作细胞质膜。
质膜可以保护细胞免受环境影响,并且充当细胞内外物质交换的守门人。当质膜承受的压力过大,无论是缺氧、营养匮乏或药物影响,质膜都会产生损伤从而导致细胞死亡。
癌细胞也同样依赖完整且功能完备的质膜生存,作为灭癌主力军的免疫细胞非常清楚这一点。比如细胞毒性T淋巴细胞(CTL)对处理癌细胞质膜有着独特的手段:分泌两种蛋白来破坏质膜和促进癌细胞死亡。

CTL分泌的穿孔素和颗粒酶是可以合作产生细胞毒性的毒素蛋白。穿孔素能够在质膜上形成孔洞,颗粒酶可以充当蛋白水解酶的作用,从孔洞进入癌细胞诱导细胞产生程序性死亡。
然而,逃避细胞死亡是癌细胞特有的标志之一。尽管CTL的策略是完备的,但癌细胞却仍然在一些人身上发展起来。《科学》的新研究发现,癌细胞并不会在CTL的攻势下乖乖投降,它们是可以对CTL的行为发起反击的。

借助高分辨率成像和活细胞功能分析,来自美国基因工程技术公司基因泰克(Genetech)的研究团队发现,癌细胞产生的内体蛋白分选转运蛋白(ESCRT)能够用来防御CTL两种蛋白的进攻。它能够修复穿孔素在质膜上产生的孔洞,以此来拖延颗粒酶进入细胞内部的时间,甚至完全阻止它们进入。
根据他们的观察,穿孔素释放后,有大量的ESCRT被精确地招募到了CTL的结合位点上。这说明癌细胞是非常有目的性地对CTL开展防御措施。
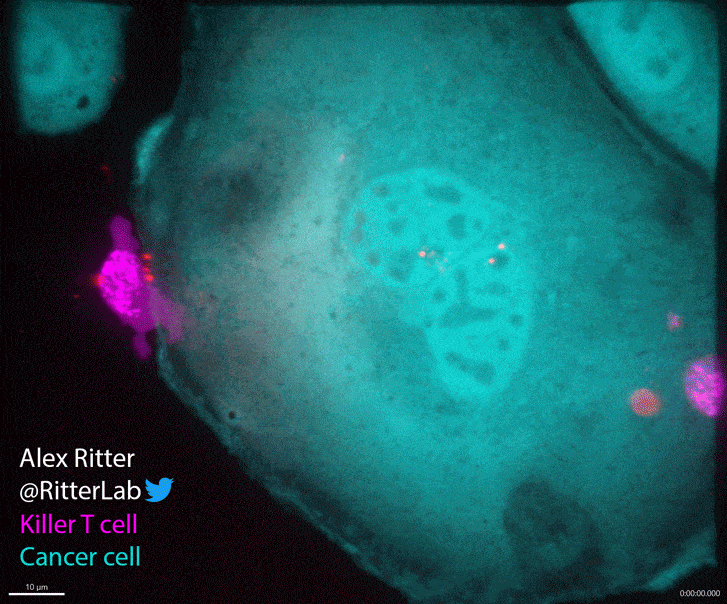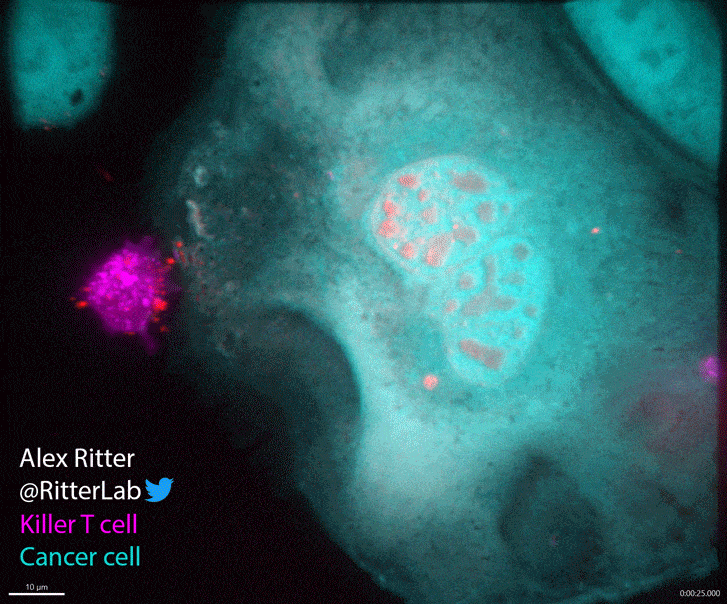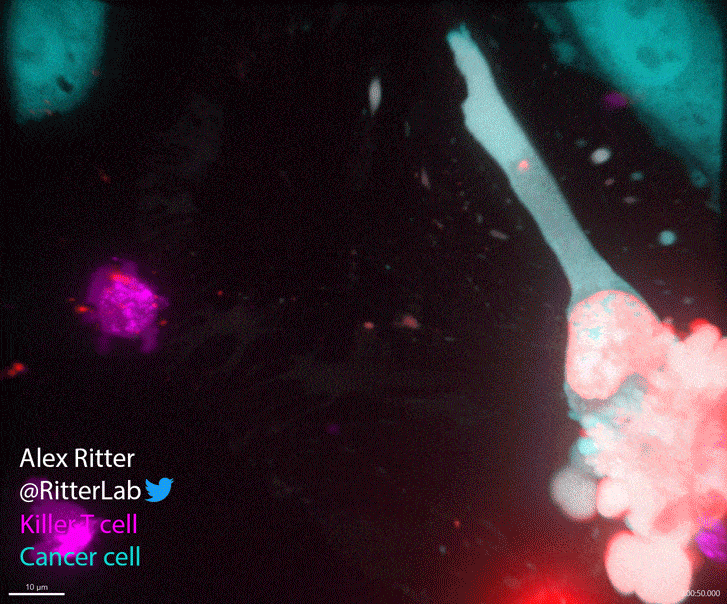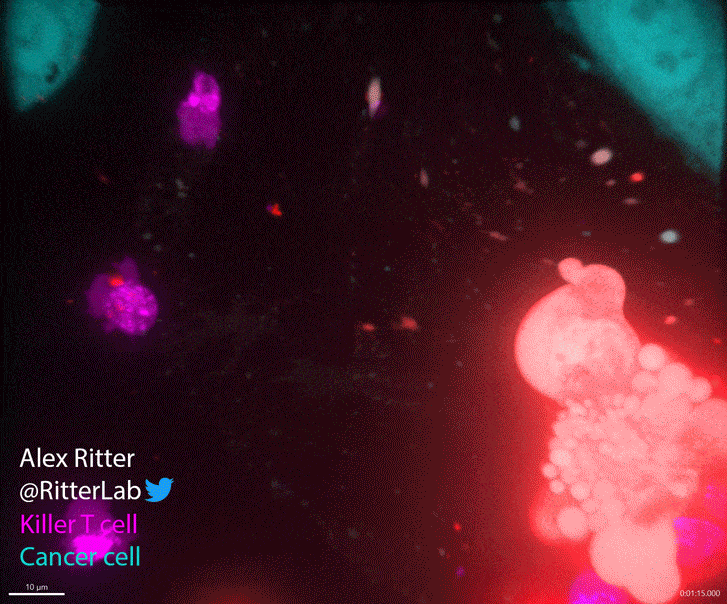
▲CTL攻击癌细胞时的实时画面,玫瑰色代表了它们正在分泌毒性蛋白(图片来源:参考资料[1],credit:Alex Ritter)
ESCRT其实在正常的细胞中也会发挥作用,但通常都是参与调节细胞死亡过程的。由于质膜随时可能会经历各种压力损伤,因此ESCRT就充当着保护和修复质膜的角色。
它们能够及时抑制质膜损伤带来的细胞凋亡,挽救正常细胞。如果ESCRT相关信号通路持续受到抑制,细胞也是会死亡的。
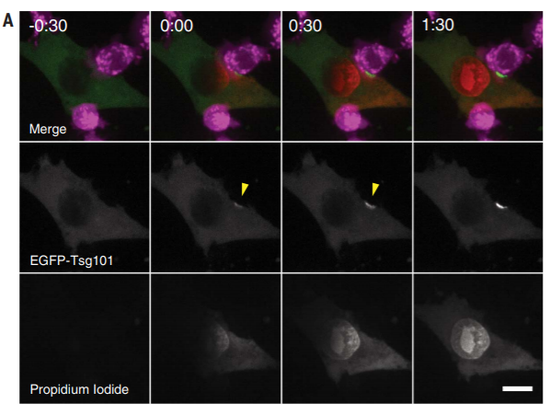
只是在癌细胞中,这种天然挽救策略成了它们保命的法宝。研究者借助CRISPR技术敲除了癌细胞中ESCRT通路的Chmp4b基因,这样ESCRT的部分功能会缺失,而这些癌细胞可以更容易地被CTL给杀死,它们对CTL攻击的敏感性显著上升。
荷兰拉德堡德大学医学教授Peter Friedl没有参与此项研究,但他指出新研究创新地借助成像技术和分子干预揭示了穿孔素和质膜修复的一个关键机制。
“ESCRT可能能成为免疫疗法改进的一种潜在目标,根据他们的研究,仅仅调整了ESCRT的功能,就使得免疫细胞的肿瘤杀伤效率提升了2-3倍,” Friedl教授表示,“干扰ESCRT的功能,很可能可以成为一种新型靶向疗法,增强CTL造成损伤的能力。”
参考资料:
[1] Preventing Attacked Cancer Cells from Repairing Membranes May Enhance Immunotherapy。 Retrieved Apr 24th, 2022 from https://www.genengnews.com/topics/cancer/preventing-attacked-cancer-cells-from-repairing-membranes-may-enhance-immunotherapy/
[2] Plasma membrane repair protects tumor cells against killer T cell assault。 Retrieved Apr 24th, 2022 from https://www.eurekalert.org/news-releases/949943
[3] ESCRT-mediated membrane repair protects tumor-derived cells against T cell attack。 Science (2022), DOI: 10.1126/science.abl3855