 正在凋亡的癌细胞。图片来源:美国国立卫生研究院(NIH)
正在凋亡的癌细胞。图片来源:美国国立卫生研究院(NIH)而就在今天,日本国立癌症研究中心报告了一种更令人意想不到的癌症传播方式,而这也是首次发现宫颈癌的母婴传播。在这2例传播事件中,癌细胞的母婴传播导致新生儿在出生后发展出了肺癌,在接受治疗后好转,但2位母亲却不幸逝世。
撰文 | 罗丁豪
本周四,日本国立癌症研究中心报道了2例宫颈癌母婴传播事件。在这2例传播事件中,初生婴儿的母亲在生育时均未意识到自己已患宫颈癌,而婴儿在出生后逐渐发展出了肺癌。案例以简报的形式,刊登在《新英格兰医学杂志》上。据该简报,这是全球首次观察到宫颈癌的母婴传播,且其传播方式和性质对医学界来说都是极为有用的信息。
第一例案例中,在男婴出生前7个月,婴儿的母亲曾筛查过宫颈癌,结果为阴性。但在婴儿得到癌症诊断、母亲再次检测宫颈癌时,结果则为宫颈鳞状细胞癌阳性。婴儿在23月大时出现了持续2周的咳嗽症状。胸部计算机断层扫描(CT)显示,婴儿左右肺的气管中出现了几个阴影团。在发现异样后,医生立刻对婴儿进行了肺部活组织检查,并在肺部组织中发现了神经内分泌癌(neuroendocrine carcinoma)。
第二例案例中的病人则是一名男孩,男孩的母亲在生育时曾筛查出宫颈息肉,但该肿瘤呈良性,医生评估其转移风险不大,因此允许婴儿正常出生。男孩在6岁时因胸部疼痛而入院检查。医生在检查时,发现男孩的左肺中存在阴影。进一步分析表明男孩患有肺部黏液腺癌(mucinous adenocarcinoma)。
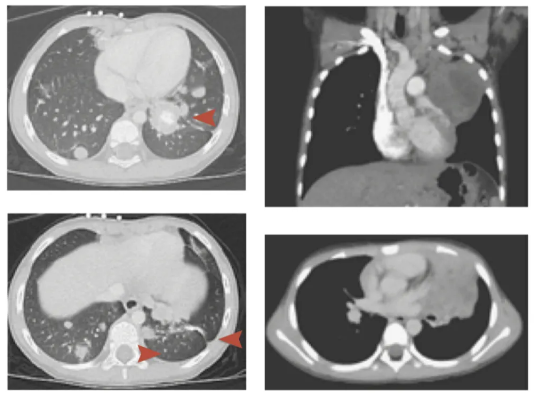 左、右2列分别为病例1和病例2中的胸部成像。左列图中红色箭头标示了病例1肺部的癌细胞群。图片来源:Arakawa et al., NJEM
左、右2列分别为病例1和病例2中的胸部成像。左列图中红色箭头标示了病例1肺部的癌细胞群。图片来源:Arakawa et al., NJEM极为罕见的传播方式
母婴癌症传播极为罕见,且传播通常由血液作为介质。2004年,一名29岁的女性在怀胎29周时诊断出了B细胞淋巴癌,随后,8个月大的婴儿也诊断出了相同的癌症。负责调查该事件的研究人员在报告中表示,婴儿体内的淋巴癌和过往报道的许多母婴传播淋巴癌一样,都是由血液传播的。这名母亲和婴儿都不幸死于癌症。根据2018年的一项统计,平均每1000例出生中就有1例涉及患癌母亲,而平均每50万例这样的出生事件中,才有一例母婴癌症传播——也就是说,平均5亿次生育中才会出现一次这样的案例。
但在本次肺癌事件中,论文的第一作者荒川歩医生指出,与其他母婴癌症传播事件不同,这2个案例中的肺癌很可能源自“含有肿瘤细胞污染的阴道液体”。在出生后的呼吸中,婴儿碰巧将含有肿瘤细胞的液体吸入了肺部,这些来自母亲宫颈的肿瘤细胞迅速在新生儿的肺部扎根生长。这样的案例虽然罕见,但正如荒川歩医生所说,我们应当告知患有宫颈肿瘤的母亲,她们身上的肿瘤细胞可能脱落并污染阴道液体。
需要注意的是,如果这2个案例中的23月婴儿和6岁男孩只是单单诊断出了肺癌,医生是无法在肺癌和他们母亲的宫颈癌之间建立联系的。幸运的是,在医院例行执行的下一代基因测序(next-generation sequencing)中,研究人员发现2位母亲和她们孩子的癌症组织十分相似:在对114个癌症相关基因的测定中,他们发现孩子癌细胞中出现的突变,与他们母亲癌细胞中存在的突变十分相似。例如,第一例病例的肺癌细胞中出现了与其母亲的癌细胞相同的KRAS基因变异;KRAS基因是典型的原癌基因(proto-oncogene),其变异与癌症紧密相关。
进一步分析揭示了“破案”的关键线索:孩子的癌细胞中不含Y染色体,而他们的生殖细胞(作为与癌细胞的对比)中却正常包含了Y染色体。这意味着,2名肺癌儿童的癌细胞很可能来自于女性;更重要的是,孩子的癌细胞中含有人类乳突病毒(Human Papillomavirus,简称HPV)。据一项发表于《病理学杂志》的研究统计,99.7%的宫颈癌都由感染HPV造成,2名儿童母亲的宫颈癌也不例外。
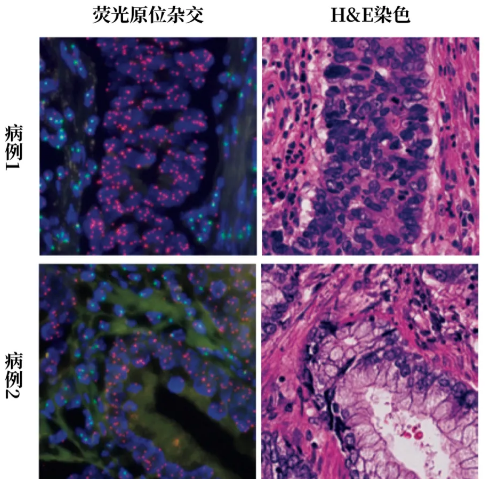 病例1、2的许多肺癌细胞只带X染色体(荧光原位杂交图像中标记为粉色)。图片来源:Arakawa et al., NJEM,翻译制图:罗丁豪
病例1、2的许多肺癌细胞只带X染色体(荧光原位杂交图像中标记为粉色)。图片来源:Arakawa et al., NJEM,翻译制图:罗丁豪结合前后3项证据,医生作出了诊断:孩子们的癌细胞极有可能源自他们的母亲。
治愈肺癌
在2名儿童的肺癌获得正式诊断后,下一个问题就是治疗。
确诊于23个月的婴儿在确诊后的一年内并未接受治疗:婴儿的母亲在孩子确诊后,坚持让医生不为婴儿治疗,而只是定期回到医院进行检查。幸运的是,在异体癌症细胞的入侵下,机体会自动以排异免疫反应(alloimmune response)抗击来自外界的细胞。因此,当母亲将孩子送往日本国立癌症研究中心时,孩子的肺癌已有好转,然而癌症细胞仍在孩子的气管内堆积。医生为孩子开具了5轮顺铂(cisplatin)和伊立替康(irinotecan)治疗与2轮卡铂(carboplatin)和依托泊苷(etoposide)治疗。但在多轮药物治疗后,孩子的肺癌仍然存在。因此,医生决定紧急采用正在进行临床试验的免疫疗法:纳武利尤单克隆抗体(nivolumab)治疗。纳武利尤单抗属于免疫检查点阻断剂(immune checkpoint inhibitor)的一种。
要想在人体内顺利繁殖,癌细胞就要躲避人体的免疫攻击。大部分癌细胞都因此演化出了抑制免疫系统的能力。在这些能力中,最有用的莫过于激活人体免疫系统自带的“关闭按钮”——免疫检查点。典型的免疫检查点包括CTLA4、PD-1和PD-L1,这些检查点蛋白一旦激活,就会抑制免疫反应。在正常的人体内,这些免疫检查点能防止免疫系统攻击人体自身的细胞。但癌细胞利用了这一点,通过激活这些检查点蛋白,使人体免疫系统对癌细胞的出现“不闻不问”,这才助长了癌细胞的泛滥。
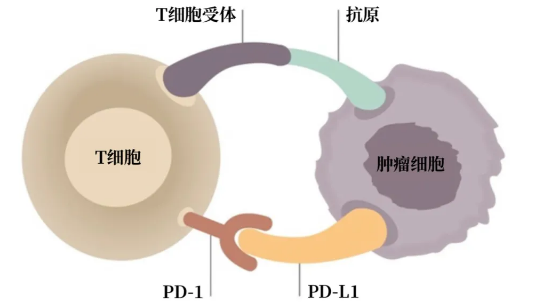 作为免疫系统的关键细胞,T细胞会表达PD-1受体;肿瘤细胞能演化出激活PD-1受体的能力,从而逃避免疫反应。图片来源:Fuereder, memo,翻译制图:罗丁豪
作为免疫系统的关键细胞,T细胞会表达PD-1受体;肿瘤细胞能演化出激活PD-1受体的能力,从而逃避免疫反应。图片来源:Fuereder, memo,翻译制图:罗丁豪因此,治疗癌症的一个好方法则是不激活这些“关闭按钮”。以PD-1为例,这是一个表达在免疫细胞表面的蛋白。如果能在癌症患者体内,用药物将PD-1“挡住”,不让癌细胞激活PD-1,就可以保持免疫系统的一部分正常功能,让免疫细胞向癌细胞进攻。纳武利尤单抗就是这样的药物。
在接受了4轮纳武利尤单抗治疗后,第一个病例的肺癌开始缓解。在14轮纳武利尤单抗治疗和肺叶切除术(lobectomy)后,第一个病例的肺癌已被完全清除,并在其后12个月内再未复发。然而不幸的是,孩子母亲的癌症已大面积转移,免疫疗法也无力挽救其生命。母亲于5个月后逝世。
第二个病例中,6岁男孩的母亲在确诊宫颈癌2年后逝世。男孩在接受传统药物疗法后出现了癌症缓解,但肺癌在停药3个月后于男孩的左肺中复发。随后的多轮药物治疗未显示出较好疗效,医生只好为他实施了全肺切除术(pneumonectomy)。在术后15个月的随访中,男孩的肺癌都未再复发。
防患于未然
宫颈癌细胞能从子宫内脱落,进入血液、羊水或阴道液体中,增加新生儿的吸入、患癌风险。在发表于《新英格兰医学杂志》的论文中,荒川歩医生等人写道:“鉴于患宫颈癌的女性中,顺产会带来母婴肿瘤传播的风险,剖腹产应变为宫颈癌母亲的推荐生产方式。”
但在一项采访中,美国癌症协会HPV相关癌症研究的高级主任黛比·萨斯洛(Debbie Saslow)和得克萨斯大学的妇科癌症学家香农·内维尔·韦斯廷(Shannon Neville Westin)表示了反对意见。她们认为,在更改临床建议前,学界需要更多宫颈癌通过顺产发生母婴传播的案例数据。
萨斯洛指出,很多日本人“对HPV疫苗持敌对态度”,“由于一些未经证实的质疑,日本出现了大规模的疫苗接种率下跌。”HPV疫苗接种项目的失败本身已足以导致宫颈癌患病率上升。萨斯洛还表示,她得知“日本的宫颈癌筛查率非常低。”所有这些因素,都可能是造成了本次报告的2例病例的“凶手”。因此,在进一步确定宫颈癌的母婴传播风险前,我们或许可以通过加大筛查宫颈癌的强度,来预防这类传播事件的发生。