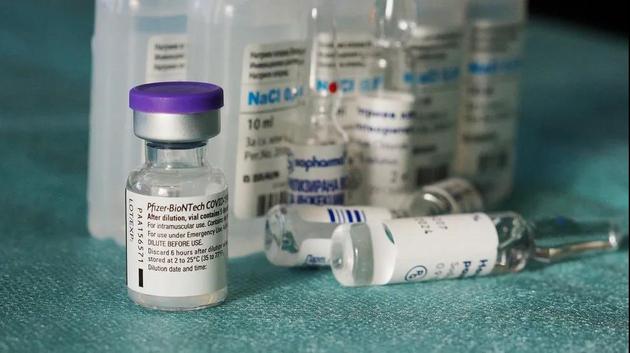
 癌细胞(扫描电镜成像)。图片来源:University of Basel, Swiss Nanoscience Institute/Biozentrum
癌细胞(扫描电镜成像)。图片来源:University of Basel, Swiss Nanoscience Institute/Biozentrum抗恶性肿瘤药物(如抗PD-1药物)的出现,是癌症治疗中一道曙光,但就算是其中知名的药物——帕博利珠单抗(也称K药),也只对40%的恶性黑色素瘤患者有效,剩余患者对这一疗法具有抗性。近期,一项发表于《科学》的研究发现,粪便菌群移植有望为一些无药可救的黑色素瘤患者带来生存的希望。
撰文 | 石云雷
审校 | 吴非
一些抗癌药物如(抗PD-1药物)的出现,让科学界燃起了攻克癌症的新希望。然而无法忽视的是,由于个体差异的存在,并不是每一位患者都能呈现出良好的治疗效果。如果能改变那些治疗效果不佳的患者的免疫及生理状态,让他们更接近恢复良好的患者,或许也能获得很好的恢复。为了实现这一目标,其中一个选择就是粪便菌群移植(fecal microbiota transplantation)。而它在癌症治疗上的应用,还得从一款明星药物说起。
抗恶性肿瘤药物
2014年9月,美国食品和药品监督管理局(FDA)加速批准了药企默沙东的明星药物——帕博利珠单抗(pembrolizumab,商品名Keytruda),也称K药——用于治疗晚期和不可切除的恶性黑色素瘤(melanoma)。这款药物是一种抗单克隆抗体。PD-1全称为程序性细胞死亡受体蛋白1,由日本免疫学家本庶佑(Tasuku Honjo)首次发现,它能在T 细胞、B 细胞和单核细胞等细胞中表达。不巧的是,癌细胞会表达特异性结合该受体的配体PD-L1和PD-L2,并通过与PD-1结合,让免疫细胞误以为自己是正常细胞。值得一提的是,这一发现也为本庶佑赢得了2018年的诺贝尔生理或医学奖。
在逃避免疫反应后,癌细胞便可以继续分裂、繁殖,并向其他位点转移。这一时期的癌症已到达晚期,通常意味着抑制或清除它们的可能性很小。但如果能阻止癌细胞欺骗免疫细胞,打断两者的信号交流,人体的免疫反应或能抑制癌细胞的发展。事实证明,靶向PD-1或PD-L1、PD-L2的抗体,确实具有很好的治疗效果,而帕博利珠单抗也曾让患者看到了奇迹。
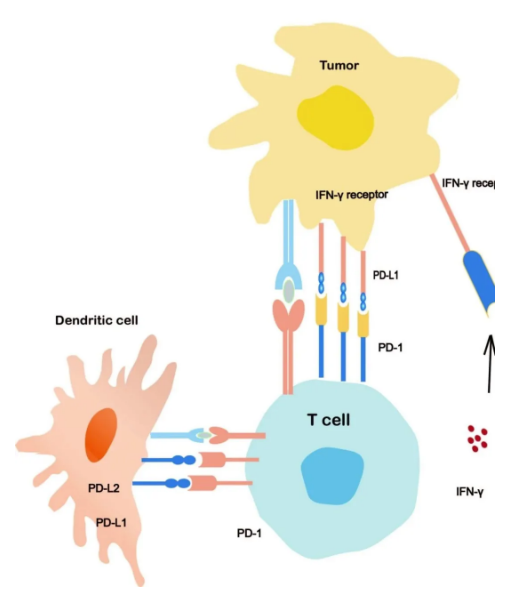 PD-1/PD-L1信号通路机制图。图片来源:《中国科学》杂志
PD-1/PD-L1信号通路机制图。图片来源:《中国科学》杂志其中一位患者是美国前总统吉米·卡特(Jimmy Carter)。2015年8月,他表示黑色素瘤已经扩散到了他的肝脏和脑部。几年前,如此严重的黑色素瘤几乎是不可治愈的。他的医生尝试了一种新的治疗方法——联合使用化疗和免疫疗法(帕博利珠单抗)。3个月后,91岁的吉米·卡特发现自己的肿瘤消失了,且他的免疫系统有望长期保护他免受黑色素瘤的威胁。2017年,FDA允许将帕博利珠单抗用于治疗任何不能切除或转移性的实体肿瘤,例如常见的肺癌、肾细胞癌和卵巢癌。
粪便移植治疗肿瘤
可惜的是,在吉米·卡特身上发生的奇迹,并未在所有黑色素瘤患者中重现。类似帕博利珠单抗的药物只对40%的患者有效,剩下的患者会对这种疗法产生抗性。随着对肠道菌群的了解加深,情况开始出现变化。研究人员发现,人体肠道中复杂的微生物组成会影响人体的免疫反应以及药物对癌症的治疗效果。
一些研究证实,通过粪便菌群移植或者给患者补充一些特定的细菌,能有效改善他们所患的肠道炎症等。去年10月,一项发表于《细胞》的研究也表示,将母亲的肠道菌群稀释后喂给剖腹产的婴儿,能降低他们患哮喘或过敏性疾病的风险。还有一些研究表明,肠道中一些关键细菌能改善抗PD-1的单克隆抗体等对癌症患者的治疗效果。
匹兹堡大学医学中心-希尔曼癌症中心和美国癌症研究所的科学家采用了相同的思路,他们尝试通过粪便菌群移植联合帕博利珠单抗治疗,增强患者对于抗PD-1疗法的敏感度,达到更好的治疗效果。而这一方法的Ⅱ期临床试验结果,近期已发表于《科学》杂志。在试验中,他们首先选择了7位粪便提供者——他们在接受帕博利珠单抗治疗后,产生了较好的效果,无病进展生存期(指从接受治疗到出现疾病进展或死亡的时间)长达56个月。
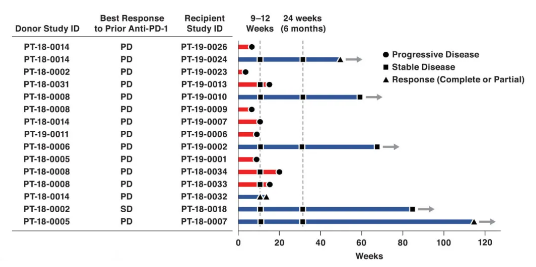 接受粪便移植后,有6位黑色素恶性肿瘤患者(蓝线)表现出病情稳定或出现了抗肿瘤免疫反应,其中1位患者由于其他原因去世。图片来源于论文。
接受粪便移植后,有6位黑色素恶性肿瘤患者(蓝线)表现出病情稳定或出现了抗肿瘤免疫反应,其中1位患者由于其他原因去世。图片来源于论文。而接受粪便移植的15位黑色素瘤患者处在另一个极端,此前包括抗PD-1疗法在内的多种疗法,对他们均没有任何效果。在粪便移植前,研究人员筛查了粪便中包括病毒、细菌、真菌和原生动物在内的共32种病原体,以保证粪便菌群移植不会导致病原菌传播。接下来,患者先接受了一次粪便菌群移植和帕博利珠单抗的联合治疗,并在后续接受了每3周一次的帕博利珠单抗治疗。
那么治疗效果如何呢?需要再次提醒的是,此前的多种疗法对这15名患者都没有任何效果。而在这次临床试验中,15名患者的整体无病进展生存期和总生存期分别为3个月和6个月,整体数据并不突出。不过值得注意的是,其中6名患者在接受治疗后,肿瘤得到了较好的控制。他们病情稳定,其中两名患者还出现了一定程度的肿瘤免疫反应。除了有一人在接受其他手术时意外去世之外,其余5人截至论文发表时仍然在世。
“复活”的免疫力
在试验期间,研究人员也收集了粪便提供者和接受者共223份的粪便样品,并利用鸟枪发宏基因学(shotgun metagenomic sequencing)技术,评估了他们的肠道菌群变化。在接受单次粪便菌群移植后,15名接受者的肠道菌群都出现了持续性变化。相比于其他患者,6名病情改善的患者的肠道菌群明显更接近提供者的肠道菌群。此外,研究中也证实此前发现的能改善抗PD-1疗法效果的细菌(如毛螺菌、瘤胃菌、双歧杆菌和红蝽菌)也在这些患者体内明显增加。
在没有出现效果的患者体内,出现了更多的髓样细胞(myeloid cell),其产生的骨桥蛋白(osteopontin)和白细胞介素8(IL-8)曾被证实与肿瘤的发展有关。而这次研究人员还发现在肿瘤位点,这种细胞会抑制能杀伤肿瘤的CD8+ T细胞的活性。与此相反,在那6名患者体内,粪便菌群移植联合抗PD-1治疗中和了这种抑制效应,并且CD8+ T细胞和CD56+ CD8+ T细胞(具有自然杀伤肿瘤的能力)的丰度都更高。这种现象也出现在那些不抵抗抗PD-1治疗和放射免疫疗法的癌症患者中。
 粪便胶囊。图片来源:Sarah L. Voisin/The Washington Post
粪便胶囊。图片来源:Sarah L. Voisin/The Washington Post匹兹堡大学的医学教授Hassane Zarour是该文章的通讯作者,他表示:“在这次试验中,抗PD-1疗法在这些患者中生效的可能性微乎其微。所以,我们可以认为任何积极的反应都归因于粪便移植。”
他和文章的第一作者、匹兹堡大学的助理教授Diwakar Davar希望能对黑色素瘤患者进行更大规模的实验。此外,他们还希望能评估粪便菌群移植是否能帮助治疗其他癌症。而在将来,一些包含有益微生物混合物的药片或能取代粪便菌群移植,以促进对癌症的免疫治疗。Zarour说:“虽然还有很多工作要做,但这一研究给基于微生物群的癌症治疗带来了希望。”恶性肿瘤正在带走无数人的性命,而对人体更全面的研究和基于此开发的新疗法,也将会延缓或阻止生命离去的脚步。
参考链接:
https://www.upmc.com/media/news/020421-Davar-Zarour-Science
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5572324/#B12
https://en.wikipedia.org/wiki/Programmed_cell_death_protein_1
文章链接:
https://science.sciencemag.org/content/371/6529/595