线粒体是细胞的能量工厂,破坏肿瘤细胞中的线粒体是抗肿瘤治疗的新策略。
中科院过程工程研究所(以下简称过程工程所)生化工程国家重点实验室与中国科学院大学化学科学学院合作,构建了光响应型颗粒剂型,实现递送光致产酸分子,在肿瘤细胞内促使大量自由基产生和大量钙离子内流,以此造成线粒体氧化应激与钙离子过载。通过上述破坏线粒体的协同机制实现肿瘤细胞的高效杀伤,在多种小鼠模型上均显著抑制了肿瘤进展,为肿瘤的高效治疗带来了新思路。
2021年11月4日,相关工作在《自然—通讯》(Nature Communications)上发表。
线粒体是细胞能量代谢的主要来源,在肿瘤发生发展中发挥着重要的作用。因此,基于线粒体破坏的抗肿瘤治疗新策略得到了越来越多的关注。科学家认为,如何在肿瘤组织内高效且特异性启动线粒体的破坏是实现安全有效抗肿瘤治疗的前提。
光激活肿瘤疗法由于具有治疗部位精确可控、毒副作用小等优点,近年来得到越来越多的研究,尤其是光照条件下还能够激活光致产酸分子释放氢离子,酸化胞内微环境。受此启发,并结合10余年抗肿瘤剂型工程的研究经验,过程工程所生化工程国家重点实验室马光辉研究员和魏炜研究员与中国科学院大学化学科学学院田志远教授进行合作,创建了负载光致产酸分子的光响应型颗粒剂型,并提出协同破坏肿瘤线粒体的治疗新策略。
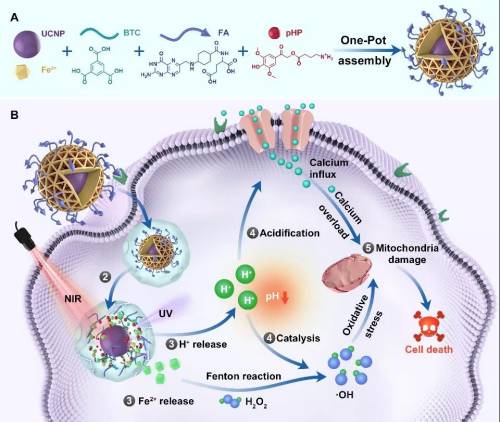 基于光响应型颗粒剂型协同破坏肿瘤线粒体的示意图(研究团队供图)
基于光响应型颗粒剂型协同破坏肿瘤线粒体的示意图(研究团队供图)研究人员将叶酸、上转换颗粒、光致产酸分子通过“一锅法”负载于金属有机框架中,形成FMUP颗粒剂型。实验证明,静脉注射后,FMUP借助叶酸分子选择性地靶向到肿瘤部位。在近红外光照射下,上转换颗粒发出的紫外光可酸化肿瘤胞内环境并释放二价铁离子,并通过芬顿反应产生更多的羟基自由基攻击线粒体。同时,胞内酸性环境还可以引起大量钙离子内流,从而导致线粒体钙离子过载。通过上述协同机制可以显著破坏肿瘤细胞内线粒体,进而高效杀伤肿瘤细胞并抑制肿瘤的生长。
上述研究已在肝癌患者来源的异种移植瘤等模型上证明了显著疗效,但仍处于动物水平的临床前研究,实际临床疗效有待进一步确认。
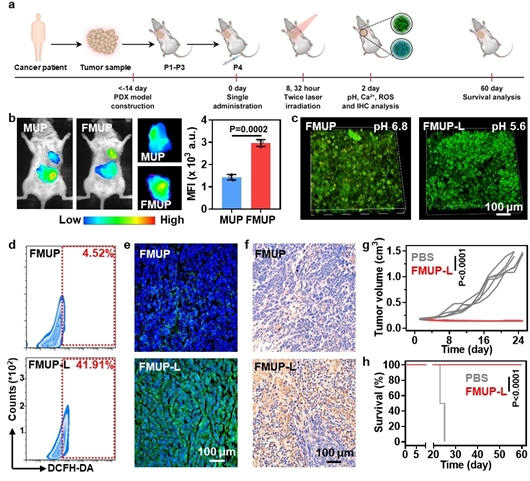
FMUP剂型在患者来源的异种移植瘤模型上的疗效评价:(a)模型的构建及治疗策略;(b)小动物成像表征FMUP在肿瘤部位的富集量;(c)光诱导肿瘤部位的酸化;(d)光诱导肿瘤部位的ROS产生;(e)光诱导肿瘤部位的钙离子过载;(f)肿瘤组织石蜡切片显示线粒体损伤相关蛋白;(g, h)小鼠肿瘤生长曲线及生存期曲线(研究团队供图)
10余年来,马光辉研究员和魏炜研究员发现和创制了一系列药物和疫苗递送新剂型,在动物模型上成功用于肿瘤、传染病、炎症性疾病的防治,并且部分剂型已通过医院伦理批准进入个体化临床前和临床研究。
博士生鲍威尔为该论文第一作者,马光辉研究员、魏炜研究员和田志远教授为共同通讯作者。该工作得到了国家自然科学基金面上项目、创新群体项目、国家重点研发计划项目和中科院战略先导科技专项的支持。
相关论文信息:
doi:10.1038/s41467-021-26655-4