原标题:基因治疗龙头蓝鸟生物股价“跌跌不休”,如何解决医药产业创新的3个关键问题
细胞治疗,是指利用患者自体(或异体)的成体细胞(或干细胞)对组织、器官进行修复的治疗方法,主要包括干细胞治疗和免疫细胞治疗。
基因治疗,则是指将外源正常基因导入靶细胞,以纠正或补偿缺陷和异常基因引起的疾病,以达到治疗目的,主要包括体内基因治疗和体外基因治疗,目前最成熟的是腺相关病毒(AAV)基因治疗。
细胞和基因治疗(Cellular and Gene Therapy,CGT)作为一种新兴技术,在近几年发展尤为迅速。据沙利文资料显示,预计2025年全球CGT市场规模为305.4亿美元,2020年到2025年预计全球CGT市场复合年增长率为71%;中国CGT市场规模预计将保持快速增长模式,2025年中国CGT整体市场规模将为25.9亿美元,2020年到2025年预计中国CGT市场复合年增长率为276%。
这其中,有一家在这个创新赛道中屹立了近三十年的基因治疗先驱——bluebird bio, Inc.(以下简称蓝鸟生物)。蓝鸟生物于2013年登陆纳斯达克市场,2019年成功获批全球首个遗传性血液病的基因治疗产品,2021年又接连获批两款产品,分别是全球首个获批的靶向BCMA的CAR-T细胞疗法Abecma以及EMA批准的首个CALD一次性基因疗法Skysona。
连续几年皆有产品获批的蓝鸟生物可谓是风光无限,然而它的股价却不断下滑。为何这家已经走到基因治疗头部的企业会出现如此反常的情况?让我们从这一切的源头技术说起。
近50年技术不断更新,FDA近期重点关注?
基因治疗和细胞治疗已经有相当长时间的发展了,它们都源自于19世纪70年代。早在1972年,Friedmann和Robin就首次提出了基因治疗的概念;1973年,Steinman和Cohn从小鼠脾脏中分离出一群胞质呈星状突起、核极不规则的细胞,命名为树突状细胞,自体免疫细胞治疗技术也由此开始发展。
几十年风雨飘摇,CGT赛道迎来过欢呼,也经历过沉寂。但在近几年,CGT赛道在技术更新、产品上市、资本看好的加持下,又迎来了蓬勃的发展。政府等相关部门也一直出台新规,规范细胞和基因治疗市场。
据不完全统计,过去一年半FDA在CGT领域就发布了《神经退行性疾病的人类基因疗法》、《COVID-19公共卫生紧急情况下许可和研究用细胞和基因治疗产品的制造注意事项》、《工业指南:在产品制造和患者随访期间测试基于逆转录病毒载体的人类基因治疗产品是否具有复制能力的逆转录病毒》、《工业指南:施用人类基因治疗产品后的长期随访》、《工业指南:用于人类基因治疗研究新药应用(IND)的化学,制造和控制(CMC)信息》等数十条相关法律法规。
成立近30年不断有牛人加入,蓝鸟生物宝刀未老?
不仅技术古早,蓝鸟生物也是一只“老鸟”。1992年4月,蓝鸟生物于美国特拉华州注册成立,其前称为Genetix Pharmaceuticals, Inc.,2010年9月更名为bluebird bio。2013年6月,蓝鸟生物登陆美国纳斯达克(NASDAQ:BLUE),发行价为17美元。成立近30年,上市8年,蓝鸟生物拥有一支庞大的管理与科研团队。
首席科学家Philip D. Gregory, D. Phil.,自2015年6月开始担任蓝鸟生物首席科学家,负责公司的科学治疗和战略研究规划。在此之前,Philip曾是锌指基因编辑垄断者Sangamo的研发副总裁,积极推动了Sangamo多个治疗领域中IND候选药物的早期发现和开发。此外,Philip还拥有牛津大学、Keble学院的生物化学博士学位,谢菲尔德大学的微生物学学士学位。
首席医学官Richard Colvin,杜克大学医学院医学博士和博士,自2021年3月起担任蓝鸟严重遗传疾病的临时首席医疗官。在加入蓝鸟生物之前,Richard是诺华公司转化医学的执行董事,在此期间他领导了一个抗感染药物的开发项目,该项目用于治疗肝炎、呼吸道感染、耐药革兰氏阴性菌感染和寄生虫感染。此外,他还曾领导了一项用于治疗听力损失的基因治疗计划。
首席bluebird Nick Leschly,普林斯顿大学分子生物学学士,沃顿商学院工商管理硕士,Nick自2010年9月起便担任该职位。此前,Nick是Third Rock Ventures的合伙人和创始成员,Third Rock Ventures是一家专注于投资生物技术初创企业的风险投资公司。Nick于2007年领导负责了两家投资组合公司的整体组建、发展和业务战略,分别是Agios Pharmaceuticals, Inc.和Edimer Pharmaceuticals, Inc.。在加入Third Rock Ventures 之前,他还曾在Millennium Pharmaceuticals工作,领导过多个早期药物项目开发。此外,Nick还创立了MedXtend公司并担任其首席执行官。
除了上述介绍的三个核心团队成员外,蓝鸟生物的其他核心成员也都具备丰富的经验,大都有在国际知名企业工作的经历以及创办公司的经历。
17个公开在研产品,四大重点关注领域
研发技术+管理技术,核心人员带领着蓝鸟生物在时间的沉淀下孕育出了基因治疗、基因编辑和癌症免疫治疗三大产品平台。
前两者是通过基因改造或基因编辑来达到从基因水平上来治疗疾病。在癌症免疫治疗产品平台基础上,蓝鸟生物根据其在基因转移技术方面的核心知识和在实施基因治疗临床试验方面的经验,建立了一个广泛而又完整的免疫肿瘤学特许专营权,旨在对患者自身免疫系统 (T 细胞)中的特定细胞进行基因改造,靶向摧毁癌细胞。
在三个技术平台的基础上,蓝鸟生物在重大遗传疾病和肿瘤学两大领域总计共有17个公开在研产品和多个未公开在研产品。在研产品适应症包括脑肾上腺脑白质营养不良、β-地中海贫血、镰状细胞性贫血、多发性骨髓瘤、成人急性髓性白血病、梅克尔细胞癌等多种遗传疾病和肿瘤。
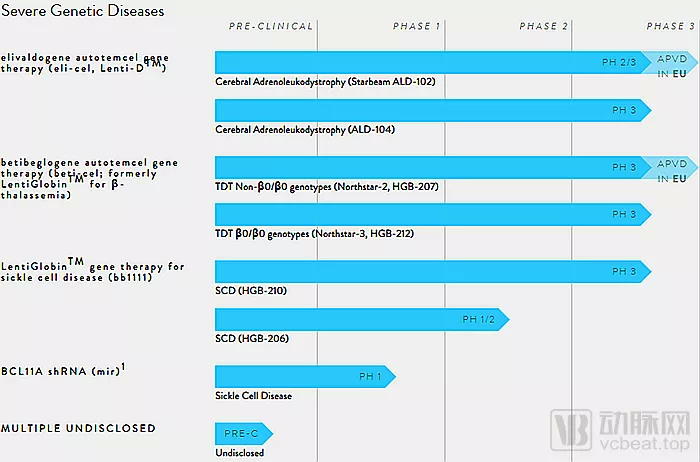 重大遗传疾病领域在研产品,图源官网
重大遗传疾病领域在研产品,图源官网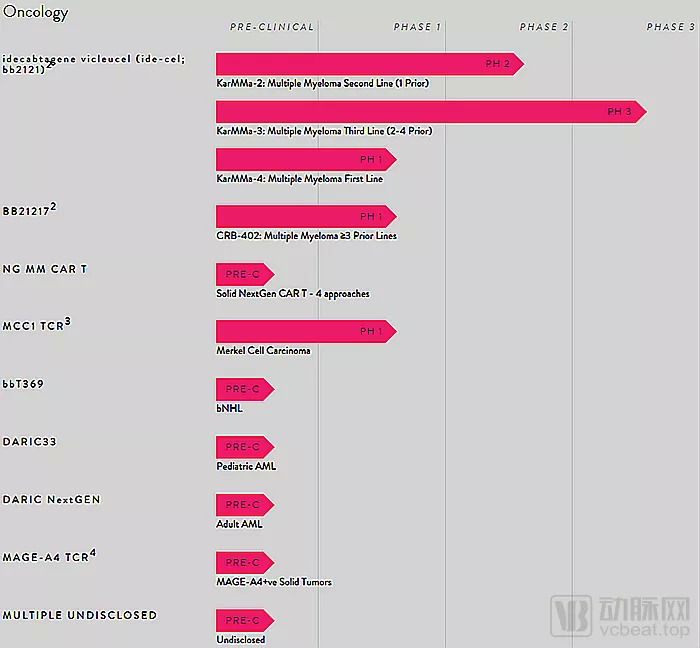 肿瘤领域在研产品,图源官网
肿瘤领域在研产品,图源官网其中,脑肾上腺脑白质营养不良(CALD)、多发性骨髓瘤(MM)、镰状细胞病(SCD)、β地中海贫血这四个领域为蓝鸟生物重点关注的疾病领域。
1、脑肾上腺脑白质营养不良:几乎只见于男性的基因突变罕见遗传疾病
脑肾上腺脑白质营养不良(CALD) 是肾上腺脑白质营养不良(ALD)的最严重表现,这是一种罕见的由ABCD1基因突变引起的遗传性疾病。值得一提的是,CALD几乎只见于男性。其中,大约40%被诊断患有ALD的男性会发展为脑ALD,脑ALD的症状通常发生在儿童早期(3至12岁)。本病发病率约为0.5/10万~1/10万,其中95%是男性,5%为女性杂合子。本病预后差,一般出现神经症状后1-3年死亡。
2、多发性骨髓瘤,占血液恶性肿瘤10%以上
血液恶性肿瘤被定义为血癌或骨髓癌,多发性骨髓瘤(MM)是世界上第二大常见的血癌,它占血液恶性肿瘤的10%以上。由于MM的特点是残留病灶持续存在以及多次缓解和/或复发,每次复发都会使患者的预后恶化,也因为复发或难治性MM对常用药物产生耐药性,所以这类患者难以得到有效治疗。在美国,大约29%的新诊断MM患者在诊断后一年内死亡,5年生存率仅约52%。根据美国癌症协会数据显示,2020年美国诊断出32,270例新发MM病例,预计将有约12,830人因此死亡。据悉,目前约有100,000名美国人患有这种疾病。
3、镰状细胞病,全球每年至少有300,000例新生患者
镰状细胞病(SCD)是一种常染色体显性遗传血红蛋白病,在全球范围内,每年约有300,000-400,000名SCD患者新生。SCD的发病率和患病率因地域而异,大多数病例发生在撒哈拉以南,如非洲、印度、中东、加勒比海、南美洲和地中海等。该病预后很差,只有约14%的患者生存至成年,如无良好的医疗条件,患者多于30岁前死亡。
4、β地中海贫血,严重患者需终身定期输血
β地中海贫血是由β珠蛋白(HBB)基因突变引起的罕见疾病,输血依赖性β地中海贫血(TDT)是该疾病最严重的形式,由于其严重贫血,所以需要终身定期输血以保持血红蛋白水平。由于长期输血会导致不可避免的铁过载,从而引发严重的并发症和器官损伤。通过基因治疗解决β地中海贫血的潜在遗传原因,有可能恢复患者自身造血干细胞正常功能,产生具有正常血红蛋白含量的红细胞,从而实现不依赖输血达到治愈疾病的最终目的。该病的发病率大约为十万分之一,发病率和流行率因地域而异,流行人群主要集中于南亚、中东、北非和南欧。
已有3个上市产品,蓝鸟就此随风而上?
从蓝鸟生物重点关注的领域,我们不难看出公司致力于攻克一些尚无有效治疗手段的、且具有一定数量级规模的重大基因疾病。因此,一旦蓝鸟生物率先获批对应的产品,将有效占领该市场的高地。
针对这些重点关注领域,蓝鸟生物目前已有3款产品成功获批上市。
2019年6月,蓝鸟生物基因疗法Zynteglo(前称:LentiGlobin,编码βA-T87Q-珠蛋白基因的自体CD34+细胞)获欧洲药品管理局(EMA)批准上市。Zynteglo是一种用于治疗年龄在12岁以上、非β0/β0基因型输血依赖性β地中海贫血(TDT)患者的基因治疗。
需要定期输血的12岁及以上患者的血液疾病,称为β地中海贫血。输血依赖型β地中海贫血是一种治疗选择有限的严重罕见疾病。研究表明,使用Zynteglo进行一次性治疗后,大多数患者不再需要输血来维持红细胞的水平,这也意味着患者在治疗的同时还可以避免定期输血带来的铁过载。
Zynteglo也成为首个遗传性血液病的基因治疗产品,该药物也因177万美元的售价而号称“全球第二昂贵药品”(仅次于诺华的Zolgensma)。蓝鸟生物在当时因此着实风光了一把。
2021年3月,BMS与蓝鸟生物合作的Abecma(idecabtagene vicleucel,ide-cel)获FDA批准上市,这是蓝鸟生物成功获批的第二款产品,更是全球首个获批的靶向BCMA的CAR-T细胞疗法,用于治疗既往接受过3种或更多种疗法(包括包括免疫调节剂、蛋白酶体抑制剂、抗CD38抗体)的复发性/难治性多发性骨髓瘤(R/R MM)成人患者。
Abecma的二期结果显示,100例疗效可评估患者的总缓解率(ORR)为72%,其中有28%的患者达到了完全缓解。在28例完全缓解的患者中,有65%的患者缓解持续至少12个月。Abecma的获批为R/R MM患者带来了一种有效、持久的创新疗法。
蓝鸟生物第三款上市的产品则是今年7月获EMA批准的Skysona(elivaldogene autotemcel,Lenti-D),用于治疗18岁以下、携带ABCD1基因突变且没有HLA匹配的同胞造血干细胞(HSC)供体可用的早期脑肾上腺脑白质营养不良(CALD)患者。Skysona是EMA批准的首个CALD一次性基因疗法,也是蓝鸟生物第二款成功获批上市的基因疗法。
Skysona利用Lenti-D慢病毒载体(LVV)进行体外转导,将ABCD1基因的功能拷贝添加到患者自身的造血干细胞(HSC)中,这些干细胞经过修饰大量的ALDP(肾上腺脑白质营养不良蛋白)酶,可以分裂以产生其它种类的血细胞来达到治疗疾病的目的。
三年暴跌92.7%,反映出生物医药产业创新的3个关键问题
成立近30年,上市也已8年,拥有庞大的科研团队和管理团队,研发管线也较为丰富,此外还有3款产品成功上市。按道理来说,蓝鸟生物的发展都应该是前路无阻的。可是,仅从股价来看,蓝鸟生物的股价从2018年3月的峰值236.17美元跌倒了今年9月初的17.14美元,三年多跌幅达92.7%!这其中发生了什么?我们可以从中汲取到哪些CGT领域发展应该注意的问题?
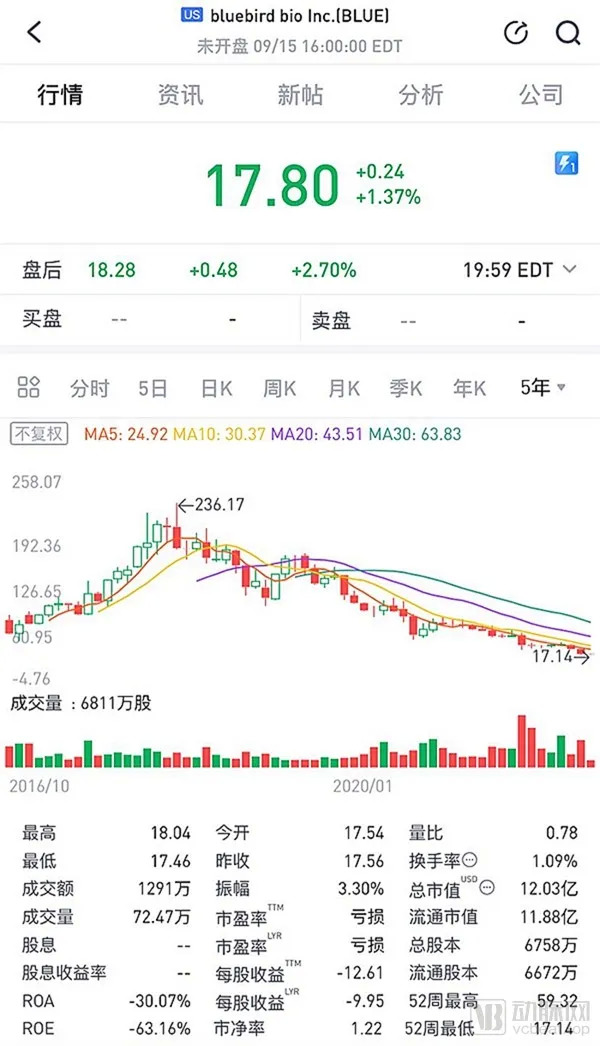 图源老虎证券
图源老虎证券先来看看最近这一两年,蓝鸟生物的股价连连下跌都是受了哪些水逆事件的打击:
2020年5月,FDA因数据不足,延迟批准蓝鸟生物与BMS联合开发的用于难治性多发性骨髓瘤患者的CAR-T疗法bb2121。
2020年11月,FDA因CMC原因,将蓝鸟生物用于镰刀状细胞贫血症(SCD)的基因疗法LentiGlobin上市申请推迟一整年。此前,LentiGlobin因为制造问题在欧洲上市也被迫推迟。
2021年2月,LentiGlobin的上市之路又遭遇了一次挫折。原因是LentiGlobin1/2期临床试验中的SCD患者分别诊断出了急性髓细胞白血病(AML)和骨髓细胞异常增生症(MDS),该药物在镰状细胞病中的I/II,III期临床研究也因此宣布暂停。由于蓝鸟生物另一款上市产品Zynteglo,与LentiGlobin临床试验使用的是同种慢病毒载体,且无法确定该事件是否与慢病毒载体相关,所以Zynteglo也因此暂停销售。
2021年4月,蓝鸟生物因未能与德国政府达成价格协议,决定将基因疗法Zynteglo暂时撤出德国市场。
2021年8月9日,由于一名患者在治疗肾上腺脑白质营养不良(ALD)的过程中出现了骨髓增生异常综合症(MDS),另外还有两名患者出现骨髓细胞异常(可能会进展为MDS),蓝鸟生物宣布暂停其治疗ALD的慢病毒基因治疗临床试验。
好坏参半,各说一头。在负面新闻满天飞的同时,蓝鸟生物仍然能够屹立不倒,得益于它也在用事实不断地证明自己。
例如,在今年2月份基因疗法LentiGlobin上市受挫后,历经一个月调查,蓝鸟生物发现用于基因治疗的慢病毒载体整合在了患者的VAMP4基因,经过分析发现并无证据表明插入到VAMP4基因会影响附近基因的调控或表达,这证明该慢病毒基因疗法不太可能引起癌症。事实得以澄清,蓝鸟生物也因此宣布将重新恢复临床试验,相关产品的销售暂停也将解封。
此外,在不断澄清和优化技术的同时,蓝鸟生物产品进度也丝毫未落。在逆境之中反而触底反弹,蓝鸟生物在今年甚至接连获批了两款产品,分别是全球首个获批的靶向BCMA的CAR-T细胞疗法以及EMA批准的首个CALD一次性基因疗法。产品接连成功上市让蓝鸟生物即使在不断负面信息的冲击下也稳坐基因治疗前排位置。
总体来讲,在这短短一两年内,曾经风光一时的蓝鸟生物像坐上了过山车,在云霄和低谷之间来回横跳,永远无法预测下一个路口是云霄还是悬崖。这体现的是蓝鸟生物这家企业的问题吗?背后体现的也许是整个创新药行业都应该注意的问题:
1.新技术的CMC建立具有挑战性
任何公司的成立,首先都会规划一条自己的CMC线路,它关乎着后续产品的安全、有效、能否成功放大生产等关键性问题。但是基因治疗在产业化领域方面很多技术都很新,并且它又是一个发展迅速的领域,这样在所难免会在现实和期望之间产生衔接的偏差。所以基因治疗CMC的建立具有一定的挑战,它可能将面临漫长复杂的制造过程、产量批量相对较低且难以扩大、发布测试繁琐等难题。
这些也许可以解释为何基因治疗的产品在研发阶段具有较好的数据,可在后续的临床以及上市过程却出现了问题。这也可以解释为何FDA在去年因为CMC问题将蓝鸟生物的基因治疗上市申请推迟一年。
2.安全:基因与细胞治疗老生常谈的问题
病毒载体是否会引发癌症、基因脱靶效应、基因编辑精准性、免疫排斥反应……这些安全性相关问题都值得我们重视,蓝鸟生物也曾因为安全问题暂停过相关临床试验以及上市产品被迫停止销售。除了技术本身的安全问题外,产业化相关的安全问题更是与企业和消费者息息相关。一个企业的基因编辑基础科研能力处于世界先进水平,不代表它在产品转换上面能够继续获得成功。产业化放大以及临床应用的过程中也需面临生产环境是否达标、样品检测是否合格、毒副性是否在可控范围内等安全问题。
3.价格与市场:临床可及性决定产品价值
除法规和CMC建立外,还有一个关乎实际应用的问题——基因治疗与细胞治疗的价格目前对于普通家庭来说的确有点“高不可攀”,造成相关产品的临床可及性较低。就连医保覆盖较完善的欧洲也在今年4月,由于蓝鸟生物未能与德国政府达成价格协议决定将基因疗法Zynteglo暂时撤出德国市场。
要如何解决价格问题,最直接的方式就是降低原材料成本,主要体现在生产所需耗材和设备方面。这也许涉及到上游材料供应商和下游材料供应商的产业链问题。选择本土化供应商也许可以解决供应周期、售后服务、供应价格等时间成本和金额成本等问题。此外,药品作为一种特殊的产品,如果无法很好地应用于临床治愈患者,那它也就失去了自身的产品价值。
写在最后
蓝鸟生物,作为一家屹立了近30年的基因与细胞治疗企业,它在发展过程中所面临的问题都是我们在探索新技术的途中会自然遇到的挫折。未来,它能否在战胜一次次意外之后仍然屹立不倒?让我们给它一些时间、给整个细胞与基因治疗领域一些时间。在合规的框架内,我们期待这项技术能够在不久的将来改写人类的健康历史。