原标题:人为什么一定会死?是什么阻止了我们长生不老?
原创 腾讯医典 腾讯医典
今天我们来讲一个很多人都好奇的话题:
人类距离实现长生不老的目标,还有多远?

 先来看看人类目前的寿命现状。过去的两百年,人类的寿命一直不断在延长,根据世卫组织统计数据,近几年全球人类平均预期寿命已经达到72岁左右,而1960年只有52.5岁。看看下图这个预期寿命走势,可以说是一路往上飙……
先来看看人类目前的寿命现状。过去的两百年,人类的寿命一直不断在延长,根据世卫组织统计数据,近几年全球人类平均预期寿命已经达到72岁左右,而1960年只有52.5岁。看看下图这个预期寿命走势,可以说是一路往上飙……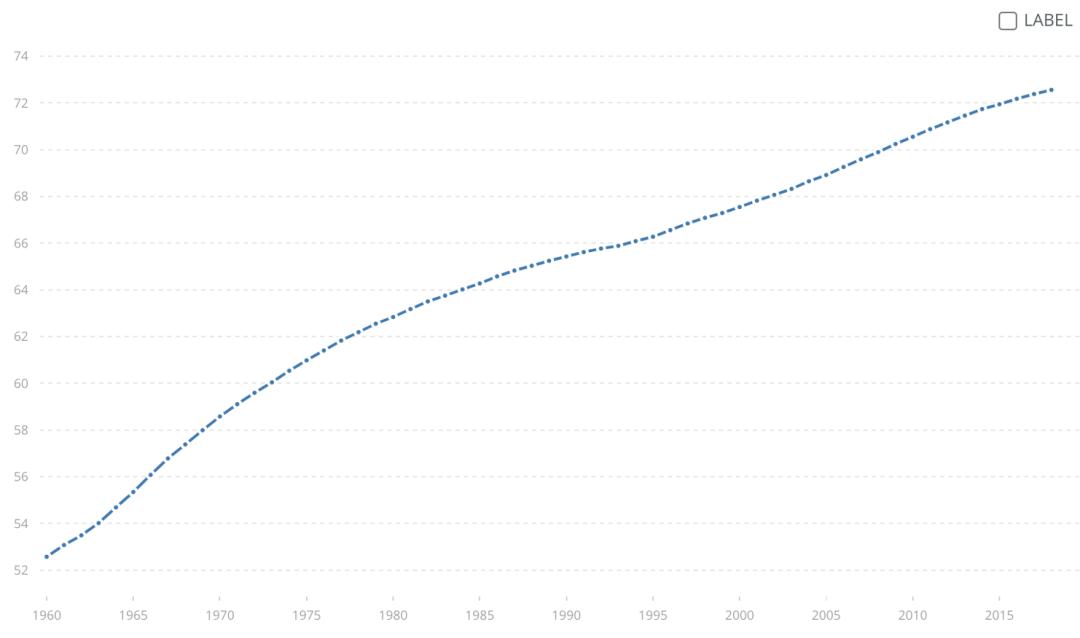 (图源:网络)
(图源:网络)但这个增长是不是无止尽呢?
实际上,人类预期寿命的增加,更多得益于人类生存环境改善和疾病防治的进步,比如癌症或心血管疾病的死亡率下降,或者儿童感染性疾病的死亡率下降[1],而不是真正做到了让人“不老”或“老得慢”。
根据已知的、比较没有争议的记录,世界最长寿的人,只有122岁[2]。
 (雅娜·卡尔曼特1875/2/21-1997/8/4图源:网络)
(雅娜·卡尔曼特1875/2/21-1997/8/4图源:网络) 很显然,是老化。
很显然,是老化。随着年龄的增长,人体内的器官必然会开始衰老……
心脏、大脑、肝脏、肾脏和骨骼肌,这些重要器官都很容易发生功能退化。 (图源:网络)
(图源:网络)除了器官,内分泌腺也会持续衰老,越来越多的内分泌激素水平降低到正常水平以下;此外肠道细胞也在老化,最终导致的结果是,老年人会出现肠道问题,尤其是120岁以上的老年人,他们的肠道几乎无法吸收营养。
因此,长生却老,换来的是低质量的生命状态,长生且保持人体的活力,才叫活着。
 (图源:《疯狂原始人》)
(图源:《疯狂原始人》) 大家都知道,人类的生长发育,是由体内细胞的分裂能力决定的。可分裂的细胞里有一种叫做端粒的特殊结构,学术界对“人为什么会衰老”这件事,提出的最著名的理论之一,就是端粒理论[3]。
大家都知道,人类的生长发育,是由体内细胞的分裂能力决定的。可分裂的细胞里有一种叫做端粒的特殊结构,学术界对“人为什么会衰老”这件事,提出的最著名的理论之一,就是端粒理论[3]。 (图源:网络)
(图源:网络)那么端粒是什么?
端粒是由一小段DNA和蛋白质构成的特殊“帽子”结构,存在于真核细胞线状染色体末端。
大家可以把它想象为鞋带末端的塑料片,就像塑料片可以保护鞋带不分叉开花一样,端粒可以防止DNA被“磨损”。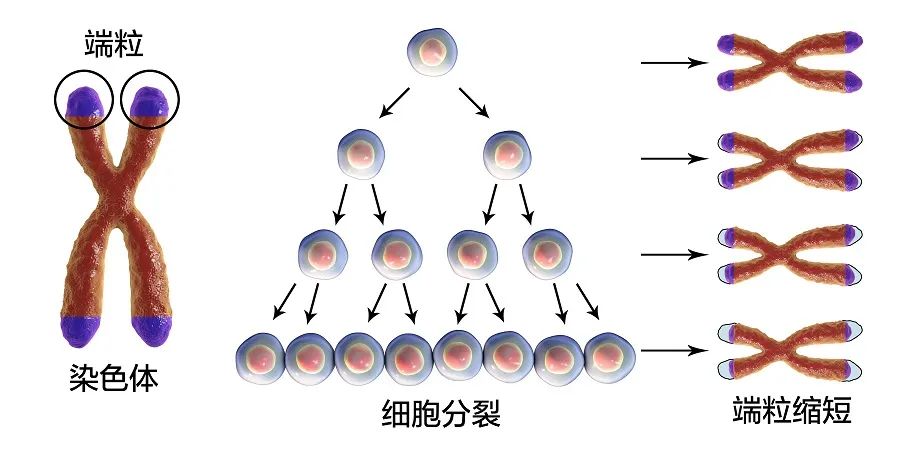 细胞每分裂一次,染色体上的端粒就被切割一次,分裂得越多,端粒就越来越短,直到它们消失时,细胞就无法再进行分裂了,然后身体的各项功能就会出现异常,衰老的进程也随之产生。
细胞每分裂一次,染色体上的端粒就被切割一次,分裂得越多,端粒就越来越短,直到它们消失时,细胞就无法再进行分裂了,然后身体的各项功能就会出现异常,衰老的进程也随之产生。端粒缩短的规律,就完全无法阻止吗?其实也不是。
细胞中还有一种叫“端粒酶”的东西,它主要负责端粒的合成、修复、延长,从而增强体外细胞的增殖能力。
换句话说,端粒的长短(生命)由它决定。
根据以上的信息,我们来开一下脑洞昂~
如果人类能保证“端粒酶”的活性,让它不断修复、合成、延长端粒,细胞持续分裂,人不就可以长生不老了吗? (图源:网络)
(图源:网络)别说,动物界真有利用这种机制“长生不老”的动物,那就是——龙虾。
 放错了图了,重新放一张。
放错了图了,重新放一张。 由于龙虾能保持端粒酶的活性,并且它的端粒酶广泛存在于所有类型的组织中,所以它们的端粒不会因细胞分裂而有所损耗[4]。这样一来,龙虾就可以“无限长大”,它们不会随着年龄的增长而减慢、变弱或失去生育能力。
由于龙虾能保持端粒酶的活性,并且它的端粒酶广泛存在于所有类型的组织中,所以它们的端粒不会因细胞分裂而有所损耗[4]。这样一来,龙虾就可以“无限长大”,它们不会随着年龄的增长而减慢、变弱或失去生育能力。 (图源:网络)相反,年龄较大的龙虾可能比年龄较小的龙虾更能生育,即使最后死亡,大多也是由于脱壳时耗能过度或感染死亡,而非死于“衰老”。
(图源:网络)相反,年龄较大的龙虾可能比年龄较小的龙虾更能生育,即使最后死亡,大多也是由于脱壳时耗能过度或感染死亡,而非死于“衰老”。 (图源:网络)
(图源:网络)是不是很刺激?
但可惜的是,与龙虾相比,在正常人体细胞中,端粒酶的活性受到相当严密的调控,只有在造血细胞、干细胞和生殖细胞等这些必须不断分裂的细胞之中,才可以侦测到具有活性的端粒酶。 (图源:网络)
(图源:网络)假如端粒酶被重新激活或者出现在了它不该出现的地方,细胞分裂可能就会失控,于是就会发生癌变……
一般来说,很多晚期恶性肿瘤不易控制,就是因为其端粒酶的激活,端粒的长度保持稳定,让癌细胞具有了持续分裂的能力[5,6]。
虽然可惜,但换个思路,如果我们能提早发现癌细胞中特异性的端粒酶,并且靶向控制住这些端粒酶,那么也可以起到抗肿瘤的作用。 除了对细胞下手,学术界还尝试过很多其他路径,说两种大家听得比较多的。
除了对细胞下手,学术界还尝试过很多其他路径,说两种大家听得比较多的。1、纳米技术
人们对纳米技术的印象,可能还来自电影《复仇者联盟4》中钢铁侠的最新战甲,但其实纳米技术在机器方面的应用还过早。 (图源:《复仇者联盟4:终局之战》)
(图源:《复仇者联盟4:终局之战》)在现实生活中,纳米技术在延缓衰老中的作用,主要是在医学美容等领域。
比如把一些具有延缓衰老功能的物质,例如抗氧化物,用纳米微粒来运输,输送到身体的特定部位,从而提高这部分器官的功能和活力。在修复人体受损器官和组织等领域,纳米技术也正在研究中[7]。
2、强大的人工智能(AI)与全脑仿真相结合[8]:
人工智能简单来说,就是让机器也具有类似人思考的能力,目前它在医学领域的应用非常广泛。
举个例子,对于人类来说,理解衰老需要对许多不同类型的数据集进行监测,例如血液检测数据或基因表达数据。这些数据集在人的生命过程中变化缓慢,在不同人群中又有着明显的差异,涉及数百万参数。
而人工智能具备强大的计算能力,可以在大量的数据中找到规律,从而提前预测人衰老的因素,帮助提出延缓衰老的解决办法。 此外,关于人工智能的研究还有一个极端设想,就是将你的意识、你大脑的思考方式,完全地转移到机器人上,等你的身体机能出现问题后,由机器人代替你继续存活,因为你的思维在,你就在。之后的你,可能就成了一个拥有人类大脑的机器人。不过,尽管这个研究方向看起来很新颖,备受科幻作品的喜爱,但现实还有很长的路要走,而且也存在一些隐私和伦理问题,比如你大脑的记忆和思考方式在刚转移给机器人时,和你的大脑是完全相同的,但随着时间的流逝,会逐渐演变出一些差异,很可能最后这个机器人就不是你了。
此外,关于人工智能的研究还有一个极端设想,就是将你的意识、你大脑的思考方式,完全地转移到机器人上,等你的身体机能出现问题后,由机器人代替你继续存活,因为你的思维在,你就在。之后的你,可能就成了一个拥有人类大脑的机器人。不过,尽管这个研究方向看起来很新颖,备受科幻作品的喜爱,但现实还有很长的路要走,而且也存在一些隐私和伦理问题,比如你大脑的记忆和思考方式在刚转移给机器人时,和你的大脑是完全相同的,但随着时间的流逝,会逐渐演变出一些差异,很可能最后这个机器人就不是你了。 总结一下,目前有许多的客观原因和技术问题,导致我们还无法实现长生不老,也没有真实存在的“长生不老药”。甚至很多抗衰老口服产品,所谓的相关实验也仅仅是在动物身上做了实验,并没有任何临床证据。
总结一下,目前有许多的客观原因和技术问题,导致我们还无法实现长生不老,也没有真实存在的“长生不老药”。甚至很多抗衰老口服产品,所谓的相关实验也仅仅是在动物身上做了实验,并没有任何临床证据。那为什么不在人身上做临床试验呢?
倒确实有些机构在做[9],但抗衰老试验这种事情,至少需要几十年才能有结论出来,所以至少目前为止,仍未直接在人体上得到过可靠的研究结果。
人类虽然没有办法实现永生,但正是因为寿命有限,我们才会无比珍惜生命。
而在有限的生命里,做更多有意义的事情,活得有价值,是比“活得长”更值得努力的。
审稿专家:罗天明 | 清华大学免疫学博士、北京大学医学部病毒学博士后、基础医学院助理研究员
参考文献
[1]GBD 2013 Mortality and Causes of Death Collaborators. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2015 Jan 10;385(9963):117-71. doi: 10.1016/S0140-6736(14)61682-2. Epub 2014 Dec 18.
[2]Jeune, B. et al.. in Supercentenarians (eds H. Maier et al.) (Springer, 2010)
https://www.guinnessworldrecords.com/news/2020/10/the-worlds-oldest-people-and-their-secrets-to-a-long-life-632895
[3]Razgonova, Mayya P et al. “Telomerase and telomeres in aging theory and chronographic aging theory (Review).” Molecular medicine reports vol. 22,3 (2020): 1679-1694. doi:10.3892/mmr.2020.11274
[4]Bowden TJ, Kraev I, Lange S. Extracellular vesicles and post-translational protein deimination signatures in haemolymph of the American lobster (Homarus americanus). Fish Shellfish Immunol. 2020 Nov;106:79-102. doi: 10.1016/j.fsi.2020.06.053. Epub 2020 Jul 28. PMID: 32731012.
[5]Trybek, T., Kowalik, A. Kowalska, A."Telomeres and telomerase in oncogenesis (Review)". Oncology Letters 20, no. 2 (2020): 1015-1027. https://doi.org/10.3892/ol.2020.11659
[6]Maciejowski, J., de Lange, T. Telomeres in cancer: tumour suppression and genome instability. Nat Rev Mol Cell Biol 18, 175–186 (2017). https://doi.org/10.1038/nrm.2016.171
[7]Ventola CL. The nanomedicine revolution: part 2: current and future clinical applications. P T. 2012 Oct;37(10):582-91. PMID: 23115468; PMCID: PMC3474440.
[8]Zhavoronkov, A., Bischof, E. & Lee, KF. Artificial intelligence in longevity medicine. Nat Aging 1, 5–7 (2021). https://doi.org/10.1038/s43587-020-00020-4
[9]Tarantini Stefano, Valcarcel-Ares Marta Noa, Toth Peter et al. Nicotinamide mononucleotide supplementation rescues cerebromicrovascular endothelial function and neurovascular coupling responses and improves cognitive function in aged mice. [J]. Redox Biol, 2019, 24: 101192.